作用原理:聚丙烯酰胺凝膠具有網絡結構和分子篩效應。它有兩種形式:天然聚丙烯酰胺凝膠和變性聚丙烯酰胺凝膠。
在蛋白質的非變性聚丙烯酰胺凝膠電泳中,蛋白質可以保持完整,并根據蛋白質的分子量、蛋白質的形狀和附著在其上的電荷量在梯度上逐漸分離;在非變性聚丙烯酰胺凝膠電泳中,脫氧核糖核酸以雙鏈狀態遷移,其流動性受堿基組成和序列的影響。

在變性聚丙烯酰胺凝膠電泳中,蛋白質變性劑——通常是SDS(SDS-PAGE),核酸變性劑通常是尿素、甲酰胺等。所以它的分離只取決于分子量。蛋白質的SDS-PAGE技術是沙博理在1967年首次建立的。他們發現,在樣品介質和丙烯酰胺凝膠中加入離子洗滌劑和強還原劑(SDS是十二烷基硫酸鈉)后,蛋白質亞基的電泳遷移率主要取決于亞基的分子量(電荷因子可以忽略不計)。
Acr聚合只能在自由基存在的情況下發生,這需要催化誘導劑系統來產生自由基,如過硫酸銨-temed(四甲基乙二胺)和核黃素-temed。前者經歷化學聚合,而后者經歷光聚合。在化學聚合過程中,引發劑TEMED加速了過硫酸銨自由基的形成,使Acr單體轉化為自由基態,導致聚合。溶液的酸堿度對聚合很重要,因為如果酸堿度太低,沒有足夠的堿來加速催化反應,太多的氧分子會很快停止聚合。因此,當制備凝膠時,在加入過硫酸銨之前,必須除去混合物中的空氣。核黃素催化的聚合常用于制備濃縮凝膠,因為用這種方法制備的凝膠孔徑較大。核黃素在光照射和微量氧存在下產生自由基聚合Acr。
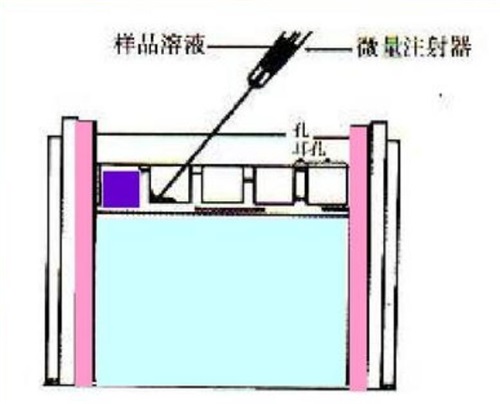
聚丙烯酰胺凝膠電泳是以聚丙烯酰胺凝膠為載體的一種區域電泳。凝膠由丙烯酰胺和交聯劑N,N-亞甲基雙丙烯酰胺聚合而成。聚丙烯酰胺凝膠電泳利用電泳和分子篩的雙重作用來分離物質。
當Acr和Bis單獨存在或混合存在時,它們是穩定的,但是當它們具有自由基體系時,它們可以聚合。引發自由基團有兩種方法:化學方法和光化學方法。化學法的引發劑為過硫酸銨(Ap),催化劑為四甲基乙二胺(Temed)。光化學法用核黃素代替過硫酸銨作為光敏物質,在紫外線照射下引發自由基。使用不同濃度的Acr、Bis和a
TEMED將它們聚合成不同孔徑的凝膠。因此,可以根據分離物質的大小和形狀選擇凝膠濃度。
聚丙烯酰胺凝膠電泳可分為兩種類型:圓盤電泳和垂直平板電泳,但它們的原理完全相同。垂直板狀因其薄板、冷卻、高分辨率、操作簡單、便于比較和掃描等優點,被大多數實驗室采用。





 微信
微信
 13287008007
13287008007